Бензойная кислота (в виде триэтаноламинной соли)
Содержание:
- Общая информация
- Безопасность и метаболизм млекопитающих
- Использует [ редактировать ]
- Безопасность и метаболизм млекопитающих [ править ]
- Производство
- Опасность
- ссылки
- токсичность
- История
- Свойства
- Ароматические вещества в шампунях
- Применение
- Применение
- производство
- Производные[править | править код]
- Реакции
- Применение
- Область применения муравьиной кислоты
Общая информация
С точки зрения химии добавка Е-210 — это карбоновая кислота, относящаяся к классу простейших одноосновных кислот ароматического ряда. Химическая формула бензойной кислоты: C7H6O2 (C6H5COOH).
С физической точки зрения бензойная кислота представляет собой кристаллический порошок белого цвета с характерным запахом. Добавка Е-210 плохо растворима в воде, из-за чего вместо бензойной кислоты чаще всего применяется бензоат натрия (пищевая добавка E-211). В то же время добавка Е-210 достаточно хорошо растворима в диэтиловом эфире и этаноле.
Впервые бензойная кислота была получена методом сублимации в 16 веке из росного ладана (бензойной смолы). Отсюда бензойная кислота и получила своё название. В 1832 году немецким химиком Юстусом фон Либихом была определена структура бензойной кислоты, а также исследованы ее свойства и связь с гиппуровой кислотой. В 1875 были обнаружены и изучены антигрибковые свойства бензойной кислоты, в результате чего она долгое время применялась при консервировании фруктов.
В промышленности добавку Е-210 получают методом окислением толуола (метилбензола) при участии катализаторов. Этот процесс использует дешевое сырье и считается экологически чистым.
Бензойная кислота хорошо всасывается организмом человека и в виде гиппуровой кислоты (взаимодействуя с белковыми соединениями) выводится через почки. Существуют обоснованные опасения, что пищевые добавки Е-210 и E-211 могут вступать в безалкогольных напитках в реакции с аскорбиновой кислотой (витамин С, добавка E-300) с образованием свободного бензола, который является сильным канцерогеном. Поэтому рекомендуется избегать употребления напитков, в которых содержаться эти добавки одновременно.
Безопасность и метаболизм млекопитающих
Выводится как гиппуровая кислота. Бензойная кислота метаболизируется бутират-КоА лигаза в промежуточный продукт, бензоил-КоА, который затем метаболизируется глицин N-ацилтрансфераза в гиппуровую кислоту. Люди метаболизируют толуол и бензойная кислота, которая выделяется в виде гиппуровая кислота.
Для людей Всемирная организация здоровьяс Международная программа химической безопасности (IPCS) предполагает, что предварительная переносимая доза составит 5 мг / кг массы тела в день.Кошки имеют значительно более низкую толерантность к бензойной кислоте и ее соли чем крысы и мышей. Смертельная доза для кошек может составлять всего 300 мг / кг массы тела. Устный LD50 для крыс — 3040 мг / кг, для мышей — 1940–2263 мг / кг.
В ТайбэйПроведенное в 2010 году в городе Тайвань медицинское обследование показало, что 30% сушеных и маринованных пищевых продуктов содержат бензойную кислоту.
Использует [ редактировать ]
Бензойная кислота в основном расходуется при производстве фенола путем окислительного декарбоксилирования при 300-400 ° C:
- C 6 H 5 CO 2 H + 12О 2 → С 6 Н 5 ОН + СО 2
Требуемая температура может быть снижена до 200 ° C путем добавления каталитических количеств солей меди (II). Фенол можно превратить в циклогексанол , который является исходным материалом для синтеза нейлона .
Прекурсор пластификаторов править
Бензоат пластификаторы , такие как гликолевых, diethyleneglycol- и триэтиленгликоль, сложные эфиры получают путем переэтерификации из метилового эфира бензойной кислоты с соответствующим диолом . Альтернативно эти частицы возникают при обработке бензоилхлорида диолом. Эти пластификаторы используются аналогично пластификаторам, полученным из эфира терефталевой кислоты .
Прекурсор бензоата натрия и связанных с ним консервантов править
Бензойная кислота и ее соли используются в качестве пищевых консервантов , представленных номерами E E210 , E211 , E212 и E213 . Бензойная кислота подавляет рост плесени , дрожжей и некоторых бактерий . Его либо добавляют напрямую, либо создают в результате реакций с его натриевой , калиевой или кальциевой солью. Механизм начинается с поглощения бензойной кислоты клеткой. Если внутриклеточный рН изменяется до 5 или ниже, анаэробной ферментации из глюкозы черезфосфофруктокиназа снижается на 95%. Таким образом, эффективность бензойной кислоты и бензоата зависит от pH пищи. Кислые продукты и напитки, такие как фруктовый сок ( лимонная кислота ), газированные напитки ( углекислый газ ), безалкогольные напитки ( фосфорная кислота ), соленые огурцы ( уксус ) или другие подкисленные продукты, консервируются бензойной кислотой и бензоатами.
Типичные уровни использования бензойной кислоты в качестве консерванта в пищевых продуктах составляют от 0,05 до 0,1%. Пищевые продукты, в которых может использоваться бензойная кислота, и максимальные уровни для ее применения регулируются местными законами о пищевых продуктах.
Высказывались опасения, что бензойная кислота и ее соли могут вступать в реакцию с аскорбиновой кислотой (витамином С) в некоторых безалкогольных напитках, образуя небольшие количества канцерогенного бензола .
Лекарственное править
Бензойная кислота входит в состав мази Whitfield в которую используют для лечения грибковых заболеваний кожи , таких как лишай , стригущий лишай и ноги спортсмена . Как основной компонент бензоина камеди , бензойная кислота также является основным ингредиентом как настойки бензоина, так и бальзама Фрайара. Такие продукты давно используются в качестве местных антисептиков и ингаляционных деконгестантов .
Бензойная кислота использовалась как отхаркивающее , болеутоляющее и антисептическое средство в начале 20 века.
Лабораторные исследования а также недавняя теоретическая работа показали, что производные бензойной кислоты являются многообещающими для подавления коронавируса ( SARS-CoV ).
Бензоилхлорид править
Бензойная кислота является предшественником бензоилхлорида C 6 H 5 C (O) Cl путем обработки тионилхлоридом , фосгеном или одним из хлоридов фосфора . Бензоилхлорид является важным исходным материалом для нескольких производных бензойной кислоты, таких как бензилбензоат , который используется в искусственных ароматизаторах и репеллентах от насекомых .
Безопасность и метаболизм млекопитающих [ править ]
Выводится в виде гиппуровой кислоты . Бензойная кислота метаболизируется бутират-КоА-лигазой в промежуточный продукт, бензоил-КоА , который затем метаболизируется глицин- N- ацилтрансферазой в гиппуровую кислоту. Люди метаболизируют толуол и бензойную кислоту, которая выделяется в виде гиппуровой кислоты .
Для людей, то Всемирная организация здравоохранения «s Международная программа по химической безопасности (МПХБ) предлагает временное терпимого потребления будет 5 мг / кг массы тела в сутки. Кошки имеют значительно более низкую толерантность к бензойной кислоте и ее солям, чем крысы и мыши . Смертельная доза для кошек может составлять всего 300 мг / кг массы тела. Оральная LD 50 для крыс составляет 3040 мг / кг, для мышей — 1940–2263 мг / кг.
В Тайбэе , Тайвань, исследование состояния здоровья города в 2010 году показало, что 30% сушеных и маринованных пищевых продуктов содержат бензойную кислоту.
Производство
Промышленные препараты
Бензойная кислота коммерчески производится частичное окисление из толуол с кислород. Процесс катализируется кобальт или же марганец нафтенаты. В процессе используется большое количество материалов, и он идет с высоким выходом.
Первый промышленный процесс включал реакцию бензотрихлорид (трихлорметилбензол) с гидроксид кальция в воде, используя утюг или соли железа как катализатор. Результирующий бензоат кальция превращается в бензойную кислоту с соляная кислота. Продукт содержит значительное количество производных хлорированной бензойной кислоты. По этой причине бензойная кислота для потребления человеком была получена сухой перегонкой бензоина камеди. Пищевая бензойная кислота теперь производится синтетическим путем.
Лабораторный синтез
Бензойная кислота дешевая и легкодоступная, поэтому лабораторный синтез бензойной кислоты в основном практикуется из-за ее педагогической ценности. Это обычная подготовка к бакалавриату.
Бензойную кислоту можно очистить перекристаллизация из воды из-за его высокой растворимости в горячей воде и плохой растворимости в холодной воде. Избегание использования органических растворителей для перекристаллизации делает этот эксперимент особенно безопасным. Этот процесс обычно дает около 65% выхода.
Путем гидролиза
Как и другие нитрилы и амиды, бензонитрил и бензамид может быть гидролизован до бензойной кислоты или ее сопряженного основания в кислотных или основных условиях.
Из реактива Гриньяра
Бромбензол может быть превращен в бензойную кислоту путем «карбоксилирования» промежуточного соединения фенилмагний бромид. Этот синтез предлагает студентам удобное упражнение для выполнения Реакция Гриньяра, важный класс углерод-углеродная связь образующая реакция в органической химии.
Опасность
Исследования показали, что превышение концентрации бензойной кислоты пагубно влияет на жизненно важные органы и вызывает нарушение психики. Дефицит органической бензойной кислоты приводит к болезням пищеварения, депрессии. Длительный период без этого вещества приводит к нарушению обмена веществ и анемии.
В косметике вред benzoic acid в основном сводится к появлению у некоторых людей аллергии в виде крапивницы. Это означает, что у человека повышенная чувствительность к этому ингредиенту. Следует сдать тест в лаборатории, чтобы точно знать диагноз. При подтверждении его назначается диета с ограничением некоторых продуктов.
ссылки
- Грэм Соломонс Т.В., Крейг Б. Фрайл. (2011). Органическая химия. Амины. (10го издание.). Wiley Plus.
- Кэри Ф. (2008). Органическая химия (Шестое издание). Mc Graw Hill.
- Химическая Книга. (2017). Бензойная кислота. Получено с: chemicalbook.com
- PubChem. (2018). Бензойная кислота. Получено из: pubchem.ncbi.nlm.nih.gov
- Wikipedia. (2018). Бензойная кислота. Получено с: en.wikipedia.org
- Дадачанджи, Диншоу. (18 мая 2018 г.) Химические свойства бензойной кислоты. Sciencing. Получено от: sciencing.com
- Министерство труда и социальных дел Испании. (Н.Д.). Бензойная кислота. . Международная безопасность химической документации. Получено с: insht.es
токсичность
-При попадании на кожу и в глаза могут появиться покраснения. Вдыхание может вызвать раздражение дыхательных путей и кашель. Прием большого количества бензойной кислоты может вызвать желудочно-кишечные расстройства, что приводит к повреждению печени и почек..
-Бензойная кислота и бензоаты могут выделять гистамин, который может вызывать аллергические реакции и раздражение глаз, кожи и слизистых оболочек..
-Он не обладает кумулятивным, мутагенным или канцерогенным эффектом, так как быстро всасывается в кишечнике, выводится с мочой без накопления в организме..
-Максимально допустимая доза по данным ВОЗ составляет 5 мг / кг массы тела / день, приблизительно 300 мг / день. Острая токсичность у человека: 500 мг / кг.
История
Бензойная кислота была открыта в шестнадцатом веке. В сухая перегонка из камедь бензоин был впервые описан Нострадамус (1556), а затем Алексиус Педемонтан (1560) и Блез де Виженера (1596).
Юстус фон Либих и Фридрих Вёлер определил состав бензойной кислоты. Последние также исследовали, как гиппуровая кислота относится к бензойной кислоте.
В 1875 году Сальковский открыл противогрибковый способности бензойной кислоты, которая долгое время использовалась для консервирования бензоатсодержащих плоды морошки.
Это также одно из химических соединений, обнаруженных в кастореум. Это соединение собрано из касторовые мешки из Североамериканский бобр.
Свойства
Формально это вещество является производным метана, поэтому, согласно IUPAC, его название – метановая кислота. Структурная формула муравьиной кислоты выглядит следующим образом:
Из этой формулы вытекают её основные свойства.
Кислотные свойства
Атом водорода гидроксильной группы отщепляется довольно легко даже под действием не только сильных, но и слабых оснований:
- HCOOH + H2O = HCOO— + H3O+
- HCOOH + OH— = HCOO— + H2O
- HCOOH + NH3 = HCOO— + NH4+
Это и обуславливает довольно сильные кислотные свойства этого соединения – оно является наиболее сильной предельной органической кислотой. Это означает, что ей присущи все свойства, характерные для соединений этого класса. Её называются формиатами («formica» с латинского переводится как «муравей»).
Реакции по карбоксильной группе
Муравьиная кислота способна также вступать в реакции этерификации – образования сложных эфиров со спиртами:
Более того, она является единственным веществом с карбоксильной группой, которое может присоединяться к двойной связи, также с образованием сложных эфиров:
Но особенности муравьиной кислоты – это не только её кислотность. Если внимательно посмотреть на структуру молекулы, можно увидеть еще одну функциональную группу – карбонильную.
Реакции по карбонильной группе
Карбонильная группа характерна для альдегидов, а значит, рассматриваемое соединение проявляет свойства и этого класса соединений. Так, его можно восстановить до формальдегида:
Или окислить до нестабильной угольной кислоты, которая быстро отщепляет воду и превращается в углекислый газ.
Ароматические вещества в шампунях
Ароматизаторы в ингредиентах шампуня
Для приятного запаха в шампуни добавляют ароматизаторы как искусственного так и натурального происхождения. В зависимости от сырья, из которого получают ароматизаторы, они могут быть как вполне безвредными, так и достаточно токсичными.
Иногда натуральный ароматизатор может вызвать даже более неприятные последствия, чем синтетический, например приступ аллергии.
Если Вы склонны к аллергии или просто не хотите подвергаться воздействию широкого класса ароматических веществ, выбирайте средства с маркировкой «Fragrance free».
Фталаты в составе шампуня
Для устойчивости аромата в шампуни добавляют фталаты — очень вредные химические вещества — эфиры фталевой кислоты, получаемые путем окисления нафталина, которые накапливаются в организме и вызывают серьезные заболевания.
Химический состав современных шампуней достаточно сложный, он может содержать десятки наименований химических веществ и их соединений. Часть веществ могут оказаться опасными для здоровья. Для снижения опасности аллергических реакций, рекомендуем использовать натуральное мыло.
Применение
Калориметрия
Бензойная кислота используется как вещество в качестве теплового стандарта для калибровки калориметров по температуре и теплоёмкости, так как теплота кристаллизации и плавления хорошо известны и воспроизводимы.
Сырьё
Бензойная кислота служит для получения многих реактивов, наиболее значимые из них:
Бензоилхлорид, C6H5C(O)Cl, получается обработкой бензойной кислоты тионилхлоридом, фосгеном или хлоридами фосфора PCl3 и PCl5
C6H5C(O)Cl — важное исходное вещество для некоторых производных бензойной кислоты, таких как бензилбензоат, используемый как искусственный ароматизатор и репеллент.
Бензоатные пластификаторы, такие как гликоль-, диэтиленгликоль- и триэтиленгликолевые эфиры, получаемые переэтерефикацией метилбензоата с соответствующим диолом. Альтернативно эти вещества получаются действием бензоилхлорида на соответствующий диол
Эти пластификаторы используются с соответствующими эфирами терефталевой кислоты.
Фенол, C6H5OH, получаемый окислительным декарбоксилированием при 300—400 °C. Необходимая температура может быть понижена до 200 °C добавлением каталитических количеств солей меди (II). Далее фенол может быть конвертирован в циклогексанол, который служит исходным веществом в синтезе нейлона.
Консервант
Бензойную кислоту и её соли используют при консервировании пищевых продуктов (пищевые добавки E210, E211, E212, E213).
Бензойная кислота, блокируя ферменты, замедляет обмен веществ во многих одноклеточных микроорганизмах и грибках. Она подавляет рост плесени, дрожжей и некоторых бактерий.
В пищевые продукты её добавляют в чистом виде или в виде натриевой, калиевой или кальциевой соли.
Губительное действие на микрофлору начинается с абсорбции бензойной кислоты липидной стенкой клетки.
Поскольку через стенку клетки может проникнуть только недиссоциированная кислота, бензойная кислота проявляет антимикробное действие только в кислых пищевых продуктах.
Если внутриклеточный pH 5 или меньше, анаэробная ферментация глюкозы через фосфорфруктокиназу уменьшается на 95 %. Эффективность бензойной кислоты и бензоатов зависит от кислотности (pH) пищи.
Кислая пища, напитки, такие, как фруктовые соки, (содержащие лимонную кислоту), газированные напитки, содержащие в растворе (углекислый газ), безалкогольные напитки с (фосфорной кислотой), соленья (молочная кислота) и другие кислые пищевые продукты консервируются бензойной кислотой и её солями.
Принятые и оптимальные концентрации бензойной кислоты при консервации пищи 0,05—0,1 %.
Медицина
Бензойную кислоту применяют в медицине при кожных заболеваниях, как наружное антисептическое (противомикробное) и фунгицидное (противогрибковое) средства, при трихофитиях и микозах, а её натриевую соль, — бензоат натрия — как отхаркивающее средство.
Другие применения
Эфиры бензойной кислоты (со спиртами от метилового до амилового) обладают сильным и приятным запахом и применяются в парфюмерной промышленности.
Некоторые другие производные бензойной кислоты, такие как, например, хлор- и нитробензойные кислоты, широко применяются для синтеза красителей.
Применение
По внешнему виду бензойная кислота – продолговатые кристаллы белого цвета, которые имеют характерный блеск. При температуре 122 градуса по Цельсию переходит в газообразное состояние. Бензойная кислота растворима в спиртах, воде, жирах. В промышленных масштабах производится путем окисления толуола. Помимо этого, вещество получают из фталевой кислоты.
Консервант используется в хлебопекарной, кондитерской, пивоваренной промышленностях для производства следующей продукции:
- фруктовых и овощных пюре;
- безалкогольных напитков;
- ягодных соков;
- рыбных продуктов;
- консервированных фруктов, оливок;
- мороженого;
- варенья, джема, повидла;
- овощной консервации;
- маргарина;
- жевательной резинки;
- конфет и сахарозаменителей;
- деликатесной икры;
- молочных изделий
- ликера, пива, вина.
Антисептические, антибактериальные способности бензойной кислоты используют в фармакологической промышленности для производства противогрибковых медикаментов, мазей от чесотки. А специальные ванночки для стоп с применением органического соединения избавляют от чрезмерной потливости, грибка ног. Помимо этого, бензойную кислоту добавляют в сиропы от кашля, поскольку она обладает отхаркивающим свойством и разжижает мокроту.
В качестве консервирующего вещества ее используют в косметике для сохранения полезных свойств и продления срока годности кремов, лосьонов, бальзамов. Благодаря сильным отбеливающим свойствам, соединение входит в состав масок, действие которых направлено на избавление лица от веснушек, неровностей на коже, пигментных пятен.
производство
Ниже приведены некоторые способы получения этого соединения:
-Большая часть бензойной кислоты производится в промышленности путем окисления толуола кислородом, присутствующим в воздухе. Процесс катализируется нафтенатом кобальта при температуре 140-160 ° С и давлении 0,2-0,3 МПа..
-Толуол, с другой стороны, может быть хлорирован для получения бензотрихлорида, который впоследствии гидролизуется до бензойной кислоты.
-Гидролиз бензонитрила и бензамида в кислой или щелочной среде может привести к образованию бензойной кислоты и ее сопряженных оснований.
-Бензиловый спирт при окислении, опосредованном перманганатом калия, в водной среде образует бензойную кислоту. Реакция происходит при нагревании или дефлегмации. После завершения процесса смесь фильтруют для удаления диоксида марганца, а надосадочную жидкость охлаждают до получения бензойной кислоты..
-Бензотрихлоридное соединение реагирует с гидроксидом кальция, используя железо или соли железа в качестве катализаторов, первоначально образуя бензоат кальция, Са (С6H5COO)2. Затем эта соль по реакции с соляной кислотой превращается в бензойную кислоту..
Производные[править | править код]
- 2,3-дигидроксибензойная кислота (пирокатехиновая кислота)
- 2,4-дигидроксибензойная кислота (бета-резорциловая кислота)
- 2,5-дигидроксибензойная кислота (гентизиновая кислота)
- 2,6-дигидроксибензойная кислота (гамма-резорциловая кислота)
- 3,4-дигидроксибензойная кислота (протокатехиновая кислота)
- 3,5-дигидроксибензойная кислота (альфа-резорциловая кислота)
- 3-нитробензойная кислота
- 3,5-динитробензойная кислота
- Толуиловые кислоты
Солиправить | править код
Соли бензойной кислоты называются бензоатами, например:
- Бензоат аммония
- Бензоат лития
- Бензоат натрия
- Бензоат магния
- Бензоат марганца
- Бензоат меди(II)
- Бензоат ртути(II)
- Бензоат свинца(II)
- Бензоат серебра
Реакции
Реакции бензойной кислоты могут протекать либо по ароматическому кольцу, либо по карбоксильной группе .
Ароматическое кольцо
Реакция электрофильного ароматического замещения будет происходить в основном в 3-м положении из-за электроноакцепторной карбоксильной группы ; т.е. бензойная кислота является .
Карбоксильная группа
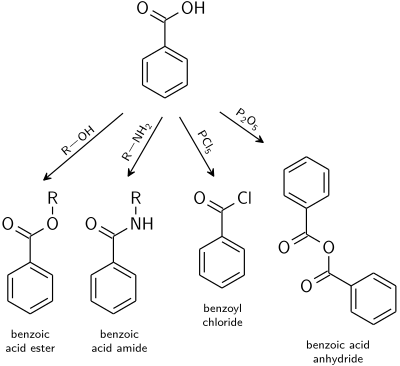
Реакции, характерные для карбоновых кислот, распространяются и на бензойную кислоту.
- Бензоатные эфиры являются продуктом катализируемой кислотой реакции со спиртами .
- Амиды бензойной кислоты обычно получают из бензоилхлорида .
- Дегидратацию до бензойного ангидрида индуцируют уксусным ангидридом или пентоксидом фосфора .
- Производные кислот с высокой реакционной способностью, такие как галогенангидриды , легко получить путем смешивания с галогенирующими агентами, такими как хлориды фосфора или тионилхлорид .
- Ортоэфиры могут быть получены реакцией спиртов в кислых безводных условиях с бензонитрилом .
- Восстановление до бензальдегида и бензилового спирта возможно с использованием DIBAL-H , LiAlH 4 или боргидрида натрия .
- Декарбоксилирование до бензола можно осуществить нагреванием в хинолине в присутствии солей меди. Декарбоксилирование Хунсдикера может быть достигнуто путем нагревания соли серебра.
Применение
Основная часть получаемой бензойной кислоты применяется в производстве капролактама и вискозы; некоторые предприятия, синтезирующих данные речовны имеют собственные мощности для получения бензойной кислоты. Также значительным является использование кислоты в производстве ее солей — бензоат: бензоата калия, натрия, кальция и тому подобное. Данные соединения нашли широкое применение в качестве пищевых и косметических консервантов, ингибиторов коррозии.
С 1909 бензойную кислоту разрешено использовать в продуктах питания, где она выполняет функции консерванта в концентрации не более 0,1%. В реестре пищевых добавок Европейского Союза бензойная кислота имеет код E210.
Бензойная кислота является сырьем для производства красителей, например, анилинового синего и некоторых антрахиноновых красителей.
Также незначительным является применение бензойной кислоты в медицине: кислота используется в изготовлении противомикробным и фунгицидным препаратов.
Область применения муравьиной кислоты
Вещество применяют в лекарственных целях, в быту и в пищевой промышленности
В малых концентрациях оно приносит большую пользу, хотя по-прежнему требует осторожного обращения
Для чего используется муравьиная кислота в медицине
Кислота в аптеках реализуется в форме спиртового раствора 1,4% в емкостях по 50 и 100 мл. Предназначена для наружного применения, обладает болеутоляющими, противовоспалительными и антисептическими свойствами. Вещество используют для:
- стимуляции питания тканей;
- дезинфекции кожи;
- расширения сосудов и капилляров;
- обезболивания, основанного на отвлекающем эффекте.
Спиртовой раствор, бальзамы и мази с содержанием вещества применяют при следующих недугах:
- невралгии;
- болях в мышцах;
- полиартрите;
- миозите;
- артралгии;
- переломах и ушибах;
- подагре;
- радикулите;
- варикозе;
- ревматизме;
- синяках, вывихах и растяжениях.
Муравьиная кислота в медицине применяется в лечении грибковых заболеваний, прыщей и угревой сыпи. Вещество в малых дозировках помогает избавиться от клещей и вшей, а также стимулирует рост волос или способствует избавлению от ненужной растительности в зависимости от дозировки.
Применение муравьиной кислоты в быту
Едкое вещество часто встречается в составе бытовых чистящих средств. Оно хорошо удаляет ржавчину, патину и известь, растворяет кальциевые отложения и цемент. Применять его можно:
- для удаления накипи;
- для чистки раковин и унитазов;
- для устранения пятен с металлических поверхностей.
Вещество добавляют в кондиционеры для белья и средства для очистки колесных дисков, в ополаскиватели для стиральных машин и посудомоек, в жидкости для ухода за ванной комнатой.
Муравьиная кислота быстро разлагается в окружающей среде и является экологически безопасной
Применение в пищевой промышленности
Пищевая добавка Е236 применяется в основном в качестве консерванта. В овощных и грибных заготовках на зиму муравьиная кислота замедляет развитие бактерий и плесени и продлевает сроки годности продуктов. Добавку можно встретить в составе маринадов для рыбы, ее используют в производстве напитков, особенно при консервации натуральных соков.
Важно! Вещество ценится в алкогольной промышленности, его дезинфицирующие свойства применяют в обработке деревянных бочек для пива и вина.
Применение муравьиной кислоты в пчеловодстве, сельском хозяйстве
Способы применения муравьиной кислоты распространяются на сельское хозяйство. Прежде всего, соединение используют для силосования, или консервирования растительного корма. Веществом в виде раствора 85% обрабатывают зеленую массу при измельчении и загрузке на транспортные средства. Кислота хорошо пропитывает корма, предотвращает развитие патогенной микрофлоры и позволяет сохранить пользу растительного сырья на всю зиму.
Практикуют также лечение пчел от варроатоза муравьиной кислотой. Опасный клещ, инфицирующий улей, препятствует расплоду насекомых, ослабляет популяцию и затрудняет сбор пыльцы и нектара. Для устранения паразита раствор с концентрацией до 85% используют так:
- средством пропитывают картонные пластинки;
- упаковывают их в пакет с несколькими дырками;
- на 2-3 недели размещают на соторамках отверстиями вниз.
Обработка пчелиных домов позволяет надежно устранить клещей, но заканчивать ее нужно за 7-10 дней до медосбора.
Для лечения варроатоза берут не более 100 мл муравьиной кислоты на улей
Ценные свойства муравьиной кислоты используют в кожевенной промышленности. Вещество применяют для дезинфекции и очистки материала, а также для однородного окрашивания при выделке и для сохранения эластичности.
В холодное время года кислотное соединение и средства с его содержанием помогают справляться с наледью. Вещество включают в состав антигололедных реагентов.